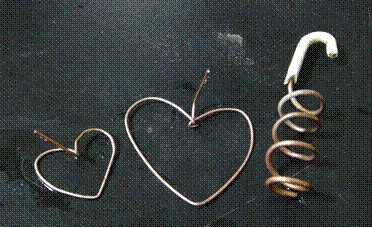發光的「銅」心 / 廖旭茂
發光的「銅」心
廖旭茂
國立大甲高級中學
教育部高中化學學科中心
[email protected]
n 影片觀賞
本影片介紹演示實驗發光胺(魯米諾)溶液在銅線的催化下,所產生的螢光反應,並在文章中介紹光化反應的原理。
影片網址:發光的「銅」心,https://youtu.be/tpX6x7XfhPw
n 簡介
發光胺(Luminol, C8H7N3O2)俗稱魯米諾,是一種白色近淡黃色的結晶粉末,是最常用的化學螢光劑之一,在鹼性的水溶液環境中,形成雙陰離子的魯米諾,遇到氧化劑(如雙氧水)產生的氧氣,反應生成激發態的3-胺基鄰苯二甲酸根離子(3-aminophthalate),隨後發出藍色螢光回到基態的3-胺基鄰苯二甲酸根離子,藍色螢光的波長為425 nm[1]。因為反應結果相當靈敏,通常用於命案現場血跡的追蹤,藉以判斷第一現場的位置,刑事鑑定上通常以氫氧化鈉配製成鹼性溶液並與雙氧水混合,當遇到血跡,血液中血紅蛋白的鐵會立刻催化雙氧水的分解,引發後續的光化學反應。本實驗參酌英國皇家化學會網站演示實驗內容[2],改以銅線為催化劑,在乙二胺四乙酸四鈉(EDTA-4Na)與氨水的鹼性環境中,觀察魯米諾溶液的光化學反應,以及因為錯合反應所造成溶液的變化。相關詳細實驗步驟及原理,分述如下:
n 藥品與器材
1. A溶液:發光胺(Luminol, C8H7N3O2,魯米諾) 0.10克、2.0 M NH3 15毫升、乙二胺四乙酸四鈉(EDTA-4Na, C10H12N2O8Na4) 0.20克。
2. B溶液:1.0 M H2O2 3毫升。
3. 同軸纜線(30公分長) 1條、單芯銅線(15公分長) 1條、培養皿 1組、濾紙(直徑9公分)1張、玻璃試劑瓶(20毫升)1個、燒杯(50毫升) 2個、玻棒1支、血清瓶(100毫升) 2個。
n 實驗步驟與結果
一、 實驗溶液配製及準備
1. 取一個50毫升的燒杯中,加入15毫升的2.0 M NH3中。接著,秤取0.10克的發光胺與0.2克的乙二胺四乙酸四鈉(EDTA-4Na)粉末,加入燒杯中,緩慢地攪拌使固體完全溶解,形成A溶液。A溶液中計約含30毫莫耳的NH3、0.55毫莫耳的發光胺、0.55毫莫耳的EDTA-4Na。另取3毫升的1M H2O2為B溶液備用,其中H2O2約計3毫莫耳。
2. 取一段約30公分長的同軸纜線,剝掉黑色的塑膠外層、網狀導電體、鋁箔及絕緣用的聚乙烯塑膠後,抽出銅線;再以尖嘴鑷子彎折出兩個大小不一的心形,備用。
3. 若有多餘的線材,可環繞鉛筆彎折成立體螺旋狀,備用;若線材不足亦可使用較粗的單芯銅線取代。圖1為彎折的銅線的式樣。
圖1:圖左方的心形是以同軸纜線彎折
二、 實驗演示
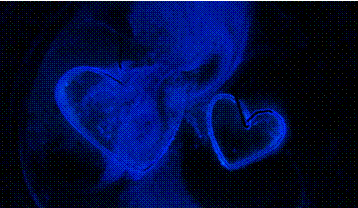
1. 演示方式一:新鮮配製完成的A、B兩溶液,緩慢地倒入一個預先鋪好濾紙的培養皿中,淹沒並覆蓋整張濾紙,隨即將兩個心形銅線放置在溶液中,觀察心形銅線周圍發生的變化;關閉電源,觀察螢光反應的發生,接著適度搖晃培養皿後靜止,觀察螢光的擴散變化。圖2和3為魯米諾在培養皿中的變化。
圖2:關燈下,出現心形螢光
圖3:反應一段時間後,心形銅線周圍溶液變為綠色
2. 演示方式二:另行配製的A、B兩溶液,緩慢地倒入一個20毫升的玻璃試劑瓶中。隨即關燈,觀察螢光發生的情形;搖晃銅線,觀察瓶中螢光的變化。當螢光轉弱時,打開電源至反應結束,觀察溶液顏色的變化。圖4~6為溶液的觀察紀錄。
圖4:立體螺旋銅線周圍出現發光胺的螢光過程
圖5:過程中立體螺旋銅線周圍出現氣泡,溶液為綠色
圖6:反應結束後,溶液轉變為深藍色
n 原理與概念
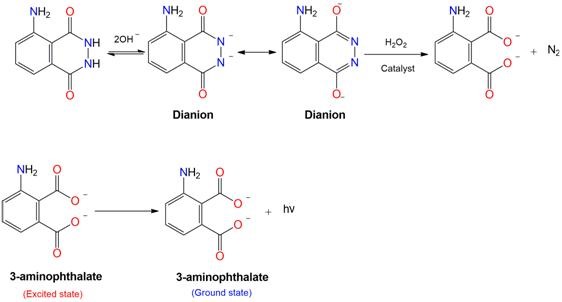
發光胺(魯米諾),為難溶於水的淡黃色粉末,化學式為C8H7N3O2,在一般的演示實驗中,多是配製兩種溶液,一種是作為氧化劑的雙氧水,另一種是將發光胺配製在氫氧化鈉或碳酸鈉存在的鹼性溶液中,其中並加入硫酸銅以作為雙氧水分解的催化劑;發光胺在鹼性溶液中會形成雙陰離子(dianion),當兩液混合時,銅離子會催化雙氧水而發生分解反應,產生氧氣[3],氧氣進而與雙陰離子反應,生成激發態的3-胺基鄰苯二甲酸根離子(3-aminophthalate),隨後發出藍色螢光回到基態[4]。圖7為發光胺產螢光的詳細反應過程。
圖7:發光胺產螢光的詳細反應過程
本實驗以銅線取代銅離子,銅線在雙氧水的氧化下,產生銅離子[5],藉由EDTA與銅離子間極高的穩定常數Kc = 1018.8,形成高穩定的螯合物[Cu(EDTA)]2−,銅離子瞬間大幅減少,進而抑制了銅離子催化雙氧水的分解速率[6][7],螢光發光時間也由傳統化學演示的30秒,延長至十數分鐘不等;光反應的區域侷限在細銅線狹窄的周圍,距離銅線越遠,銅離子的濃度越低,培養皿大部分的區域,幾無光化學反應進行,呈現一片黑暗;若搖晃培養皿,銅離子擴散開來,螢光亦隨之散開,圖8為搖晃培養皿導致發光強度更佳。
圖8:搖晃培養皿,銅離子擴散開來,催化發光胺的發光。
當玻璃試劑瓶的反應經歷一段時間後,因為螯合的Cu(EDTA)2−的生成,溶液為綠色;本實驗因發光胺為限量試劑,數分鐘後便不再發光;同時隨著EDTA-4Na的減少,未螯合的銅離子濃度升高,雙氧水的催化反應速率越來越快,實驗最後因銅離子與氨水錯合,溶液變為深藍色。
經實驗測試,其他螯合化合物,如草酸鈉等亦可像EDTA一般,抑制銅離子的催化反應,延長演示時間。
n 安全注意及廢棄物處理
n 參考資料
1. Luminol, https://en.wikipedia.org/wiki/Luminol.
2. Lighting up copper, https://eic.rsc.org/exhibition-chemistry/lighting-up-copper/2000050.article.
3. Spyridon Skounas, Constantinos Methenitis, George Pneumatikakis, and Michel Morcellet (2010). Kinetic Studies and Mechanism of Hydrogen Peroxide Catalytic Decomposition by Cu(II) Complexes with Polyelectrolytes Derived from L-Alanine and Glycylglycine. Bioinorganic Chemistry and Applications. Volume 2010 (2010), Article ID 643120, from https://www.hindawi.com/journals/bca/2010/643120/.
4. Bassam Z.Shakhashiri, Chemical Demonstrations, Vol. 1, The university of Wisconsin press (1983), p. 156-167.
5. Will hydrogen peroxide blacken copper?, http://antoine.frostburg.edu/chem/senese/101/redox/faq/h2o2-cu.shtml.
6. EDTA, http://en.wikipedia.org/wiki/EDTA.
7. 李威霖(2010)。以電解系統處理化學銅廢水研究。國立交通大學機構典藏畢業論文。參閱https://ir.nctu.edu.tw/bitstream/11536/44014/2/651603.pdf.