
臺灣化學教育
Chemistry Education in Taiwan銀奈米粒子的微量合成和鑑定
楊水平
國立彰化師範大學化學系
n 簡介
本實驗的目的是透過化學還原法來微量合成銀奈米粒子(silver nanoparticles),利用氫硼化鈉(sodium borohydride)當作還原劑,還原銀離子(Ag+)成為金屬銀(Ag)。氫硼離子(borohydride ions)也當作穩定劑用於分散銀奈米粒子,並使用PVP當作穩定劑。本實驗的微量鑑定方式有廷得耳效應、繞射、聚集、穩定和光譜分析等。為節省藥品用量和保護生態環境,本實驗採取微量實驗和一鍋合成法(one-pot synthesis);為避免用過的器材造成的污染,直接使用未用過的樣品瓶和PE滴管。
n 實驗原理
一、 奈米材料及其特徵
奈米(Nanometer, nm)是表示長度的單位或尺度,1奈米(nm)等於1微米(μm)的1/1000,也等於10‒9 m。通常,奈米用於表示原子或分子等級的粒子大小或電磁波的波長,例如:銀原子的直徑為0.288 nm,能引起尿結石的細菌最想直徑為50nm;病毒的大小範圍為20-250 nm,可見光範圍約為380-750 nm,紫外線的波長為200-380nm。奈米等級的物體肉眼和光學顯微鏡看不到,需要用電子顯微鏡才能觀察到。奈米材料就是指是指在三維度中至少有一維度處於奈米尺度(介於1-100 nm)或由奈米尺度範圍的物質為基本結構單元所構成的材料的總稱。銀的原子半徑為0.28 nm,假設銀奈米顆粒球形的直徑範圍為1-100 nm,銀原子的數量從30至3.0 × 107個原子。
奈米材料出現兩項重要的特徵。其一為表面原子數激增:與相同質量的巨觀材料相比,奈米等級材料的表面積對體積的比例激增。在1947年,第一代電晶體的尺寸在1 cm以上,在iPhone 11的Apple A13擁有85億個電晶體。現今,一個電晶體長度不到5 nm,縮小程度超過第一代約200萬倍。曾經是世界第一高樓的臺北101大樓,相當於其高度509米縮小到0.25 mm。通常較小的奈米粒子具有較高比例的表面金屬原子,導致較高的催化活性和更具化學反應性。其二為量子效應(Quantum effect):不同於巨觀世界,量化效應中能量是連續的。當材料由巨觀縮小至接近於原子或分子層次大小時,奈米的能量分布由連續轉變為量化的狀態,從而明顯地影響奈米材料的許多性質。量子尺寸效應(Quantum size effect)是由”限制”的現象所引起的,並且在10 nm或更小的奈米粒子中更為普遍發生。在塊狀材料中,電子的移動被視為波狀,並且可以“自由”在原子之間移動。當縮小粒子為奈米大小時,電子波的空間範圍與粒子的大小相當,電子開始“感覺到”粒子邊界的存在並相應地調整它們的能量。透過這種方式,電子被“限制”在量子化的能階中。奈米材料呈現出量子效應有截然不同的特性,例如:鋁等穩定的材料是可燃的,矽等絕緣體則變成導體。
以光學特性為例,當奈米粒子足夠小時,其光譜吸收能量與奈米粒子的表面有很強的耦合,尺寸在2-10 nm的奈米粒子會表現出離子化的共振效應。這是由於奈米粒子的價電子(valence electrons)當照光時激發至能量較高的導帶(conduction band),然後該價電子的能量以光的形式自發性釋放而回到穩定的價帶(valence band)。這種共振效應通常稱為表面電漿子共振(surface plasmon resonace, SPR)或局域表面等離體共振(localized surface plasmon resonace, LSPR),如圖1所示。不同粒徑的奈米粒子具有不同的能隙大小,表面電漿子共振的能量也不同。(註:開啟圖1的圖片來源網址,雙擊綠色圖示,即可觀察到表面電漿子共振現象。)
圖1:表面電漿子共振的示意圖,左上圖為面極化入射光:波長520 nm,極化方向與短軸平行;左下圖為面極化入射光:波長520 nm,極化方向與短軸垂直;右上圖為面極化入射光:波長1000 nm,極化方向與長軸垂直,步伐生共振效應;右下圖為面極化入射光:波長1000 nm,極化方向與長軸平行,發生共振效應。
(圖片來源:圖解表面電漿共振,國立中正大學,https://bit.ly/3R7txGo.)
以銀奈米粒子的光學特性為例,當金屬銀研磨成為奈米級的大小後,用肉眼可見到其顏色由本來的銀白色轉變成黃色。銀奈米粒子變為黃色是因為此奈米粒子吸收可見光(380~750 nm)中的410 nm波長(藍光),而見到其互補色(黃色),並且吸收藍光的能量與銀奈米粒子表面引起耦合而發生共振效應,使得銀奈米粒子表面的自由移動的電子雲(electron cloud)被極化,亦稱表面電漿子(surface plasmon)或稱表面電漿極化子(surface plasmon polariton)被極化,隨著光波的吸收波長而來回震盪,而發生奈米粒子的共振效應。
銀奈米粒子已廣泛應用於家用器具、醫療保健行業以及食品、環境和生物醫學,例如:在生物和生物醫學的應用抗菌、抗病毒、抗發炎、抗癌和抗癌症等。此外,銀奈米粒子有良好抗菌能力,成為使用最廣泛的殺菌奈米材料,例如:紡織品、冰箱表面和個人護理產品。一般而言,銀奈米粒子大多與二氧化鈦一起作為化學反應的催化劑。
二、 銀奈米粒子的合成
銀奈米粒子合成方法有物理和化學方法,化學方法包括:沉澱法、微乳液法、化學還原法、及電化學還原法。其中以化學還原法最為廣泛,此反應是銀離子還原成為金屬銀,例如:硝酸銀(silver nitrate, AgNO3)當作氧化劑,使用適量的硼氫化鈉(sodium borohydride, NaBH4)當作還原劑,並且用過量當作穩定劑。其反應如式[1]所示。
2AgNO3(aq) + 2NaBH4(aq) → 2Ag(s) + H2(g) + B2H6 (aq) + 2NaNO3(aq) [1]
(還原劑) (銀奈米粒子)
為節省藥品用量和保護生態環境,本實驗採取微量實驗和一鍋合成法(one-pot synthesis);為避免用過的器材造成的污染,直接使用未用過的樣品瓶和PE滴管。此外,裝在小樣品瓶內實驗畢未用完的銀奈米粒子溶液,學生可以帶回家永久保存。
三、 銀奈米粒子的鑑定
(一)廷得耳效應(Tyndall effect)
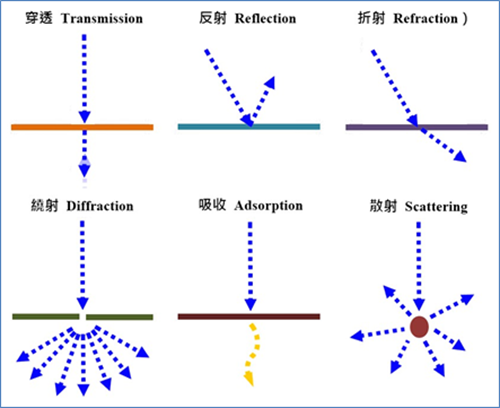
廷得耳效應(Tyndall effect)是指當一束光線透過膠體(如銀奈米粒子溶液),面相入射光的垂直方向,肉眼可觀察到膠體裡出現一條明亮光束的散射現象。若光束照射到物體的尺寸大於入射光的波長,則光線發生反射,如圖2的「反射」示意圖所示;若照射物體的尺寸小於或等於入射光的波長,則光線發生的散射,如圖2的「散射」示意圖所示。
圖二:光照射到物體的交互作用:穿透、反射、折射、繞射、吸收、散射的示意圖。
(圖片來源:楊水平,2022)
在化學上,膠體的粒子直徑(1-1000 nm)介於溶質粒子(< 1 nm)與懸浮液粒子(1000-10000 nm)之間。當可見光(波長380-750 nm)照射到膠體(或溶膠)時,可觀察到光波環繞微粒而產生明顯散射,如圖2的「散射」示意圖所示。由於真溶液(true solution)的粒子小於1 nm,以致光線的強度隨粒子體積的減小而明顯減弱,而導致對光線的散射作用很微弱,光線幾乎直接穿透,如圖2的「穿透」示意圖所示。懸浮液的粒子較膠體的粒子為大,是一種可以沉降的非均相流體,當可見光照射到懸浮液時,光線大多呈現反射,如圖2的「反射」示意圖所示,只有少部分粒子具有廷得耳效應。使用雷射筆的紅光照射銀奈米粒子溶液和硝酸銀溶液,藉由廷得耳效應可以區分真溶液、膠體或懸浮液。
圖3:銀奈米粒子(左瓶)有廷得耳效應,而硝酸銀溶液(右瓶)則無。
(二)繞射(Diffraction)
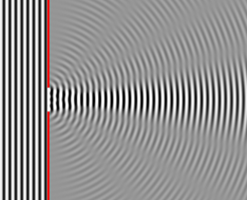
繞射(Diffraction)是指光束遇到障礙物(如光碟片)或小開口(如光柵)時發生不同程度的彎散傳播現象,形成幾何陰影區域的干涉或彎曲,如圖2的「繞射」示意圖所示。若一個障礙物的小開口放置在光源和觀察屏之間,則於觀察屏上會出現光亮區域與陰晦區域,形成明暗相間的繞射現象,如圖4所示。
圖4:紅色雷射光束穿過小圓孔後投射到觀察屏上的繞射圖案(左),來自寬度為四個波長的狹縫與入射平面波的繞射圖案(右)
(圖片來源:Diffraction, https://en.wikipedia.org/wiki/Diffraction.)
本實驗滴加銀奈米粒子溶液在透明玻璃上,乾燥後銀奈米粒子形成固體堆積物。利用雷射光照射,在暗室的觀察屏上可觀察到繞射的圓形圖案,如圖5右所示。
圖5:紅色雷射光照射到有銀奈米粒子固體堆積物時呈現較大的圓形圖案(左),而沒有銀奈米粒子堆積物呈現較小圖案(右)。
(三)聚集(Aggregation)
膠體和懸浮液分散在連續介質中,其顆粒大小的範圍在1~1000 nm之間。超過這尺寸的粒子可能從懸浮液中發生沉澱。奈米材料的尺寸範圍(1-100 nm)是在膠體和懸浮液顆粒的尺寸範圍內,這樣的粒子具有極小尺寸而導致高表面能。為降低表面能,此樣的粒子傾向發生聚集(aggregation)現象。科學家應用金奈米粒子與金屬離子混合會發生聚集的現象,透過簡單快速的比色法可檢測重金屬離子的濃度,如Cu2+、Co2+及Pb2+離子的濃度。
本實驗使用實驗當作聚集物,當銀奈米粒子溶液加入食鹽時,食鹽在水中解離的鈉離子與氫硼離子發生作用,進而造成負電荷層遭受破壞,使得溶液中的銀奈米粒子發生聚集現象,顆粒變大而沉澱析出,如圖6所示。
圖6:銀奈米粒子溶液在蠟層上形成兩顆圓球狀的液滴,左側未加顆粒狀食鹽(黃色),右側有加入顆粒狀食鹽(暗黃色)。
(四)穩定(Stabilization)
奈米粒子結構具有高表面能的熱力學不利因素。透過吸附顆粒表面周圍的穩定劑,可以分散並穩定奈米粒子的結構。適當厚度的分散層對於穩定含有高濃度奈米粒子的膠體十分重要。厚的分散劑層(穩定劑層)會導致顆粒周圍過多的排除體積,以致粒子不穩定;而薄的分散劑層,導致顆粒不穩定而發生粒子聚集。這兩種效應都會降低膠體中奈米粒子存在的最大濃度。
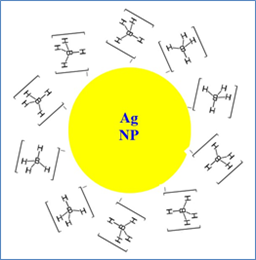
本實驗合成銀奈米粒子,使用過量的氫硼化鈉(NaBH4)當作還原劑,過量的氫硼化鈉在水中會解離出氫硼離子(BH4‒)當作穩定劑,導致銀奈米粒子均勻地分散在水溶液中。這分散的可能原因是銀奈米粒子表面的銀原子有空軌域(缺電子),氫硼離子帶負電(有多餘電子),兩者之間在銀奈米粒子的表面以靜電力相互吸引而包覆一層負電荷層;抑或氫硼離子解離成三氫化硼(BH3)和氫負離子(:H‒),:H‒有孤電子對與銀奈米粒子之間以路易斯酸鹼相互吸引而包覆一層負電荷層,形成穩定的銀奈米粒子溶液,如圖7左所示。
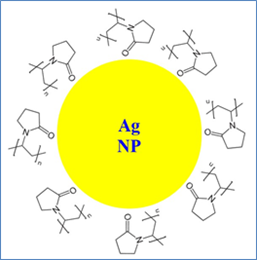
圖7:穩定劑與銀奈米粒子表面銀原子之間的作用,穩定劑為氫硼離子(左)和PVP(右),上面兩圖為示意圖,僅表示銀奈米粒子與穩定劑之間的作用,而不表示銀奈米粒子的大小與穩定劑的數量之間的關聯
本實驗也使用聚乙烯吡咯烷酮(Polyvinylpyrrolidone, PVP)當作穩定劑。PVP分散銀奈米粒子的可能原因是銀奈米粒子表面的銀原子有空軌域,PVP的氧原子帶有部分負電荷(有孤電子對),兩者之間在銀奈米粒子的表面以路易斯酸鹼相互吸引而包覆一層負電荷層,形成穩定的銀奈米粒子溶液,如圖7右所示。
(五)可見光光譜分析(Visible Spectroscopic Analysis)
透過紫外‒可見光譜儀(UV-Visible spectrometer),可測得合成銀奈米粒子的可見吸收光譜。進而找到最大吸收度的光譜波長,並且推知合成金奈米粒子直徑大小。可見光照射到銀奈米粒子溶液的吸收光譜,如圖2的「吸收」示意圖所示。
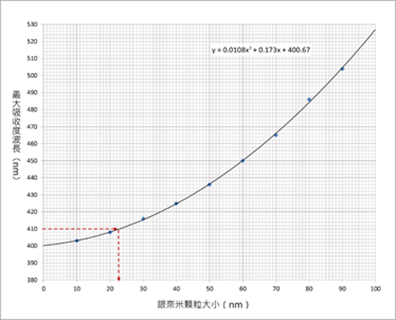
藉由文獻資料(見參考資料3)提供的銀奈米粒子不同粒徑大小的最大吸收度波長的光譜(見參考資料3),可以轉化成為最大吸收度波長與其顆粒大小的關係之趨勢線,如圖8所示。根據圖8的趨勢線,銀奈米粒子的顆粒越小,其最大吸收度的波長越短。若合成銀奈米粒子最大吸收度的波長為410 nm,則可透過趨勢線推知其顆粒大小為23 nm。抑或,藉由趨勢線的二元方程式y = 0.0108x2 + 0.173x + 400.67,若最大吸收度的波長y = 410 nm時,則其顆粒的大小x = 22.5 nm。
圖8:銀奈米粒子的最大吸收波長與顆粒大小的關係
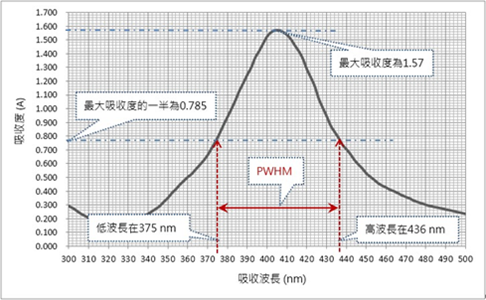
此外,藉由光譜圖的吸收度最大一半的波峰寬度(The peak width at half the absorption maximum, PWHM)可以判定銀奈米粒子大小的均一程度,PWHM越小表示奈米粒子的大小越均一。圖9為銀奈米粒子溶液的吸收光譜圖,其最大吸收度為1.57,其最大吸收度的一半為0.785(1.57/2),此吸收度與波峰有兩個交點,高波長與低波長之差即為PWHM。低波長之處在375 nm,高波長之處在436 nm,此PWHM為436 nm – 375 nm = 61 nm。
圖9:銀奈米粒子的吸收光譜PWHM
(六)電子顯微鏡圖像(Electron Microscope Image)
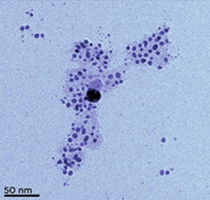
藉由電子顯微鏡(Electron microscope)的圖像,可觀察到銀奈米粒子的粒徑大小和形狀。圖10左顯示由銀離子在腐殖酸(humic acid)溶液中形成的銀奈米粒子的穿透電子顯微鏡(Transmission Electron Microscope, TEM)圖像(添加顏色是便於清楚觀察),比例尺代表50 nm,此圖像中的銀奈米粒子的大小並非均一,其粒子形狀也非全部圓形。腐殖酸傾向於吸附在奈米顆粒上(此處可見為淡淡的雲),使之分散在膠體中。圖10右顯示銀奈米粒子的掃描電子顯微鏡圖像(Scanning Electron Microscope, SEM),比例尺代表2 μm(有10格,每格200 nm),此圖像中的銀奈米粒子的粒徑大小並非均一,其粒子形狀也有很大的差異。
圖10:銀奈米粒子的穿透電子顯微鏡(左)和掃描電子顯微鏡(右)圖像
(圖片來源:Silver Nanoparticles, https://bit.ly/3B01X8t; Scanning Electron Microscope Image of Silver Nanoparticles, https://bit.ly/3Avct66.)
n 實驗步驟
一、 銀奈米粒子的合成
使用未用過乾淨的PE滴管,滴加1.5 mL(30滴)新鮮製備的0.0020 M NaBH4(硼氫化鈉)到一個3 mL的玻璃樣品瓶中,此瓶無需清潔直接使用未用過。用附特氟龍蓋,緊緊地轉緊瓶蓋。放置此樣品瓶在一個50 mL燒杯的冰水浴中,使其冷卻。取出此樣品瓶,立即打開瓶蓋。使用PE滴管,立即滴加10滴(0.5 mL)0.0010 M AgNO3(硝酸銀)到此樣品瓶中,滴加速率約1秒1滴,並且滴加時需要搖晃。滴加完畢後,緊緊地轉緊瓶蓋,立即放入冰水浴中,直到溶液變成鮮黃色,如圖11所示。(Yang, 2013)【註:(1)硝酸銀溶液不可連續滴加,否則銀奈米粒子溶液會變黑;(2)燒杯的選用不宜過大且冰水浴水位不宜超過樣品瓶的高度,否則樣品瓶難以直立。】
圖11:冷卻樣品瓶並滴加硼氫化鈉溶液直至溶液呈現鮮黃色,右圖為左圖的放大。
二、 銀奈米粒子的鑑定
(一)廷得耳效應(Tyndall effect)
使用紅光雷射筆,直接照在兩個樣品瓶中含有合成銀奈米粒子溶液和硝酸銀溶液,觀察兩種溶液是否出現一道紅光光束。其操作方式,詳見圖3。
(二)繞射(Diffraction)
取一片乾淨的玻璃片或載玻片,在此片上距離1.5 cm處分別滴加2-3滴銀奈米粒子溶液。使用電磁加熱攪拌器,以微熱狀態,放置此片在加熱板的邊緣位置,慢慢地加熱直到溶液乾燥。在暗室中,用紅光雷射筆對準並照射銀奈米粒子形成固體堆積的區域,在屏幕上觀察是否出現紅光圓點放大。同樣地,雷射光照射到沒有銀奈米粒子堆積的區域,觀察是否出現紅光放大。其操作方式,詳見圖5。
(三)聚集(Aggregation)
取1/4張A4大小的白色紙(或影印紙),使用一小塊白蠟用力地塗上一厚厚的蠟(蠟層不可有孔洞而使溶液滲透到紙張)。在蠟層上距離約1-2 cm的兩處,用乾淨的PE滴管,分別滴加2滴的銀奈米粒子溶液,形成兩個圓球狀的液滴。在其中一顆液滴,加入少量的顆粒狀氯化鈉,觀察其顏色變化,並比較與另一顆液滴的顏色。其操作方式,詳見圖6和圖12。【註:進行聚集之前,不可加入PVP穩定劑。否則,聚集不易發生。】
圖12:進行銀奈米粒子聚集試驗的兩顆圓球狀的液滴
(四)穩定(Stabilization)
為了在穩定的條件下以利保存銀奈米粒子溶液,在樣品瓶中加入5滴約3%聚乙烯吡咯烷酮(Polyvinylpyrrolidone, PVP)當作此溶液的穩定劑,蓋緊瓶蓋子並搖動混合均勻。
(五)可見光光譜分析(Visible Spectroscopic Analysis)
取一支1.5 mL乾淨的塑膠比色管,用乾淨的PE滴管,加入10滴(約0.5 mL)銀奈米粒子溶液到該管中,並用蒸餾水進行等量稀釋。利用紫外‒可見光譜儀(UV-Visible spectrometer),測定合成銀奈米粒子的吸收光譜。透過吸收光譜,找到最大吸收度的光譜。然後,藉由最大吸收度的光譜,推知銀奈米粒子的粒徑大小,詳見圖8。再來,透過製作PWHM,推知自己合成的銀奈米粒子的均一程度,並與別人或他組比較是否較佳,詳見圖9。【註:(1)若已加入PVP穩定劑,則不必加入蒸餾水稀釋;(2)測量吸收光譜後,銀奈米粒子溶液可倒入樣品瓶中。】
(六)電子顯微鏡圖像(Electron Microscope Image)
依照穿透或掃描電子顯微鏡的操作手冊,自己實際操作或由熟悉儀器操作者操作電子顯微鏡。取得圖像後,觀察到銀奈米粒子的粒徑大小和形狀。【註:這實驗是可選的,視學校的設備而定。】
n 教學提示
l 教學時間分配:(1)講解實驗原理和實驗步驟:約20-40分鐘;(2)實驗操作時間:合成方面:約5-10分鐘,鑑定方面:約30-50分鐘(不含電子顯微鏡圖譜的鑑定)。合計時間約55-100分鐘,教師可依照學生的程度,安排教學時間的長短。
l 本實驗可與另一實驗由作者編寫的「金奈米粒子的微量合成和鑑定」合併,上課時間約100-150分鐘(不含電子顯微鏡圖譜的鑑定),可在3小時的實驗課完成。
l 教學流程:本實驗的教學流程可為先解說實驗原理再操作實驗,或先操作實驗(包含合成和鑑定步驟說明)再解說實驗原理。前者為傳統實驗室教學,後者為學生先做實驗對實驗變化現象產生好奇,進而激發學生對科學知識的學習興趣和渴望。
l 上課地點與對象:本微量實驗的操作容易,實驗用器材和配製溶液集中在置物箱,可帶到教室或室外讓國高中學生操作實驗。作者曾經指導學生在教室進行實驗,實施方便且順利。針對國中生,鑑定方面只做容易操作的廷得耳效應、繞射、聚集及穩定;針對高中生,鑑定方面可增加一項光譜分析。
l 硝酸銀價格:有一家商家販賣純度99%,1,260元╱25 g;18,375元╱450 g。有一家電商販賣(未標示純度),15,015元╱500 g;另一家電商販賣0.1 M溶液(試藥級),280元╱100 mL,280元╱500 mL。配製100.0 mL 0.0010 M硝酸銀,用0.017 g,以15,015元╱500 g計,其價格約0.5元;每位學生或每組花費0.0026元;以280元╱500 mL計,其價格約0.56元;每位學生或每組花費0.0028元。其實,本微量實驗硝酸銀的花費單價很低。教師可考慮實驗藥品兩倍用量,增加學生攜帶回家成品的用量。
l 樣本瓶價格:容量3 mL,一盒100個,有臺灣商家販賣一盒價格2,500元,每個25元;有一家境外電商販賣3 mL,一盒100個,新台幣500元,每個5元。兩家價格差異很大。若經費短缺且希望學生攜帶自己的實驗作品回家永久保存,教師可選購便宜的樣本瓶。
l 在合成金奈米粒子之後立即加入穩定劑PVP,可穩定期溶液而不易使之聚集而變黑。但是此舉不利於進行銀奈米粒子的聚集實驗。為成功完成實驗,教師指導學生時應該特別注意實驗步驟的附註。
l 實驗操作時,請學生注意安全防護,必須穿實驗衣、戴乳膠手套和安全眼鏡。
n 參考資料
1. Shui-Ping Yang, Microscale Synthesis and Characterization of Silver Nanoparticles in the Teaching Laboratory, 15th ACC (Asian Chemical Congress) Poster, No. 1318, Singapore, Augest 25-27, 2013.
2. Diffraction, https://en.wikipedia.org/wiki/Diffraction.
3. Silver Nanoparticles: Optical Properties, https://bit.ly/3QXDwxv.
4. Silver Nanoparticles, https://bit.ly/3B01X8t.
5. Scanning Electron Microscope Image of Silver Nanoparticles, https://bit.ly/3Avct66.
6. 圖解表面電漿共振,國立中正大學,https://bit.ly/3R7txGo.
7. 楊水平。金奈米粒子的微量合成和鑑定。臺灣化學教育。第48期,8月,2022。http://chemed.chemistry.org.tw/?p=42346。
n 學生實驗講義
下載學生實驗講義PDF檔—「銀奈米粒子的微量合成和鑑定」














Please give us your valuable comment