設計適合國小學生動手做的化學實驗:
在臺灣小學高年級實施現況分析
周正秋1,3,*、張自立2、辛懷梓2
1國立臺北教育大學自然科學教育學系碩士在職專班
2國立臺北教育大學自然科學教育學系
3臺北市立大安區仁愛國民小學
[email protected]
■前言
在十二年國民基本教育課程綱要自然科學領域課程手冊初稿中的新舊課綱學習內容的對照表裡提到:在自然界的組成與特性的課題中學習內容Ina-III-1物質是由微小的粒子所組成,而且粒子不斷的運動。九年一貫課程綱要安排在第四學習階段之認識物質,以及次主題120物質的組成與功用第三學習階段物質可以分解與組合實施。新課程綱要則將此課程內容調移到第三學習階段實施,但以物質可以分解為更小的粒子,不必提及原子的概念(教育部,2017)。
目前的自然領域教材在國小六年級上學期關於「熱對物質的影響」的課程裡安排了多項實驗,如物質受熱後可以恢復原狀或無法恢復原狀的變化、物質三態皆有熱漲冷縮的現象、熱的傳播方式…,對於剛進入自然領域教學的菜鳥「老」老師–我而言,大多只能按照課本中的內容來進行教學活動,剛開始我會擔心面對學生在課堂上的臨時提問答不出來的窘境,因此在上課前便會將廠商提供的教師手冊、教師專用課本一看再看。即使在教過一年(7個班級)之後,對於教材與教法也只是處在較為熟稔的階段。
去年9月有幸進入國北教大自然教育研究所就讀,在化學特論周老師的課堂上,接觸到美國中學的化學教材,它的第一章就是在探討物質–固態、液態和氣態,因此萌生了想要把該章節中與六上「熱對物質的影響」有關的內容加入我的課堂教學之中的想法。在翻譯第一節分子重要性的過程中,讓我感受到臺灣與美國教材的差異,一開始便讓學生知道這個章節的重點概念是什麼,讓學生透過各種有系統的活動操作,從中去觀察、去紀錄自己看到的現象為何?如何解釋這種現象?並試著提出自己的看法。同時在教學過程中能利用現代的科技–網路媒體資源,讓學生能具體的體現水分子的各項活動。
因此,筆者試著將美國中學的化學教材(第一章第一課分子問題的教材內容翻譯,融入在自然課程康軒版國小六年級上學期的第二單元熱對物質的影響教學內容中來實施。希望藉由這樣的教學活動讓六年級學生對於物質的組成與特性能有更進一步的認識。
■物質的組成是什麼?
物質是一個科學上沒有明確定義的詞,一般是指靜止質量不為零的東西。物質也常用來泛稱所有組成可觀測物體的成份。所有可以用肉眼看到的物體都是由原子組成,而原子是由互相作用的次原子粒子所組成,其中包括由質子和中子組成的原子核,以及許多電子組成的電子雲。一般而言科學上會將上述的複合粒子視為物質,因為它們具有靜止質量及體積。原子本身並非靜止不動,而會因溫度影響不斷做熱運動(振動)。物質中的原子由於電力的作用而產生鍵結,此鍵結使得原子間會保持在某一特定的平均距離(穩定距離),當原子間距太近時會有排斥力,太遠時則會產生吸引力(信望愛文教基金會,2017)。
美國物理學家費曼在教學時使用的《物理學講義》(The Feynman Lecture on Physics) 第一冊第一章曾說:假如由於某種大災難,所有的科學知識都弄丟了,只有一句話可以傳給下一代,如何才能使用最少的詞彙來傳達最多的訊息?就是:「所有的物體都是由原子所構成。」(科學園,2010)
表一有關物質的三態的微觀解釋
|
物質
|
金屬的晶體結構及混合物
|
化合物
|
|
組成
|
物質由同類原子或不同類原子聚集而成
|
物質由同類原子或不同類原子結合而成
|
|
成因
|
原子之間主要以電磁力的交互作用,使彼此間維持適當的距離。原子不停地運動著,當彼此略微離開時會相互吸引,而當彼此靠近時則會相互排斥。
|
例如:兩個氧原子結合成為一個氧分子,或兩個氫原子與一個氧原子結合成為一個水分子。原子之間形成化學鍵,將分子內的原子束縛成為一定的形狀,但原子不停的振動,動態地維持一定的平均距離。
|
|
固態
|
a.固體內的原子呈現規則的排列。
b.原子在各自的平衡位置附近作凌亂無序的微小振動,這種原子的運動現象與溫度有關,稱為熱運動。
c.當溫度不高時,在電磁力的強力束縛下,原子間無法產生結構性的改變,故固體有一定的體積及一定的形狀。
|
a.在熔點以下的溫度時,物質呈現固態。
b.原子與分子形成排列整齊的晶體結構並維持一定的相對位置。
c.原子與分子僅能在其排列位置上振動而不能自由移動,因此固體有一定的體積及一定的形狀。
|
|
液態
|
a.溫度升高時,原子的熱運動加劇,振動現象變得較為激烈,原子可以掙脫在固定位置上的束縛,此時固體將熔化成為液態。
b.液體有一定的體積,但沒有一定的形狀。
|
a.溫度高於熔點、又低於沸點時,物質呈現液態。
b.分子內原子的振動速度增大,分子的運動速度也增大,打破晶體結構的束縛,使分子可以自由移動,但分子間仍有電磁力的約束,使相鄰分子間仍保持一定的平均距離。
c.液體有一定的體積,但沒有一定的形狀。
|
|
氣態
|
a.溫度再升高時,原子的振動更為激烈,可以掙脫彼此間的束縛,每個原子可以不受拘束的自由運動,此時的狀態稱為氣態。
b.氣體沒有一定的體積,也沒有一定的形狀。
|
a.溫度高於沸點時,物體呈現氣態。
b.分子的平均運動速度甚大,使得分子間不再相互束縛,每個分子皆可自由運動,因此氣體沒有一定的體積、也沒有一定的形狀。
c.分子內的每個原子不斷在振動,分子也在快速的移動與旋轉,與器壁發生碰撞時產生壓力。當溫度增高時,分子的運動速度增大,即可使氣壓增大。
|
資料來源:科學園高中物理(高一)Chap2-1物質由原子所組成。
■本課程實驗器材
一、每組的材料:小杯水、滴管、兩根冰棒棍、蠟紙、2張大型的索引卡(5×8”)、膠帶
■教學流程
壹、準備活動(引起動機)
1. 討論一下化學和物質
你可以透過簡短的討論來開始上課。詢問學生他們的想法–關於化學的研究可能是甚麼。你可以感受到學生以前的知識,找出一些迷思概念,並試圖讓學生在“同一層面”。告訴學生化學是研究關於物質及其作用為何的一種學習。你也可以這麼說,化學是關於物質如何在一個非常小的狀態下產生作用的研究。詢問學生,地球上常見的三種物質型態(固體,液體和氣體)。
(1) 向學生提問如下,以引導他們的思考:
•什麼是物質的一些例子?
告訴學生,物質被定義為有質量並占有空間的任何物品。以水為例繼續討論。
•水是否有質量,是否佔用空間?
一桶水是非常重的。它天生就有質量,它也佔用桶子的空間。由於它有質量和占用空間,所以水是一種物質。但是,這只是一開始,在化學方面,我們想要更深入地了解物質是如何形成和如何作用的。
(2) 給每個學生一個活動表
學生將記錄他們的觀察結果並回答有關活動表上的相關問題,不論是以一個班級、分組或單獨的方式來完成,完全取決於教學者的指示。他們可以原子和分子來解釋它或者採取進一步的部分活動表來完成,並且可以從活動手冊的教師版本中發現問題和答案。
貳、發展活動
l 探索
1.設計一個活動來探索水分子間彼此的引力
在這個活動中學生仔細觀察一滴水及其在蠟紙上移動的情形,他們會看到水滴很容易聚在一起卻不容易分開的現象。目的是要讓學生開始思考關於水或是任何實體,在分子水平上得到水分子彼此間互相吸引的結論,產生這些吸引力的原因會在後面章節中討論。
進行問題調查
水是否容易結合在一起?
每組材料
裝水的小杯子、滴管、2根冰棍棒、蠟紙(wax paper)、2張大的索引卡片(5×8”)、膠帶
教師準備
用蠟紙將索引卡完全覆蓋住,並在蠟紙邊緣處用膠帶固定,為每組準備兩張卡。
操作步驟
(1) 使用滴管輕輕擠壓出一滴水,但不要讓這滴水完全從滴管中落下。在不讓懸掛在滴管上的水掉落下來的狀態下,看看你可以移動多遠。
(2) 將4或5滴水放在蠟紙上,使它們聚集成一滴中等尺寸的水珠。
(3) 輕輕地將蠟紙向不同方向傾斜,以使上述活動中的水珠移動。
(4) 使用你的冰棒棍在蠟紙上慢慢移動你的水珠,並嘗試使用你的冰棒棍將水珠分成兩個。
(5) 用你的冰棒棍將兩滴水珠移近彼此。只要移動其中之一,就可以讓兩滴水珠合一。
3.紀錄和討論學生的觀察
在回答後續問題活動之前,讓學生有時間記錄他們的觀察結果。一旦他們開始回答問
題,必須以整組的方式來進行討論。
(1) 當你從滴管中擠出一滴水時,水是否破裂?還是在一起的?
(2) 當你傾斜蠟紙時,水珠是分散或是在一起的?
(3) 當你在蠟紙上拉起水珠時,水珠看起來是聚合在一起還是容易分開的樣子?
(4) 當你試圖分開你的水珠時,它很容易被分開嗎?
(5) 當兩滴小水珠碰在一起時發生了什麼事?
預期結果
當蠟紙傾斜或移動時,水珠會堆在蠟紙上並保持在一起的型態,要把這樣的水珠分成兩個是很困難的。當水珠一接觸到彼此,便會快速且容易的結合在一起。
|
|

|
|
圖一:從滴管中擠出一滴水珠
|
圖二:試著讓水珠不掉落
|
|
|
|
|
圖三:將一滴水珠移近另一滴水珠
|
圖四:兩個水珠聚合成一個較大的水珠
|
4.做一個實驗證明水分子是在運動
材料
高透明塑料杯、室溫水、白紙、食用色素(紅色,藍色或綠色)
步驟
(1) 加室溫水至杯中,大概到3/4杯。
(2) 讓學生仔細觀察,當你添加一到兩滴食用色素到水杯時,別太快,讓顏色慢慢地混入水中。
(3) 拿起杯子,並在杯子後面放上一張白紙,讓學生更容易看到顏料在水中移動和混合的情形。
預期結果
一滴食用色素會慢慢移動並混入水中,最後所有的杯子中的水分會被均勻著色。
詢問學生
你的觀察如何支持水分子正在移動的想法?
幫助學生理解,由於水分子移動並將顏色向各個方向推動,因此食用色素混入水中,同時食用色素本身的分子也正在運動。
注意:在美國中學化學教材第五章中,學生將會知道水分子和著色分子對彼此是相互吸引的。這些吸引力也有助於解釋水中顏色的混合。
l 說明
5.展示在液態水中顯示分子的動畫。
顯示液體的分子模型動畫粒子。
www.middleschoolchemistry.com/multimedia/chapter1/lesson1#particles_of_a_liquid
解釋一下,小球是代表水分子,讓學生知道,現在,你將使用圓或球來表示分子和原子,但最終他們會使用更詳細的模型。現在,學生應該關注分子的運動,它們如何相互作用,以及它們之間的距離。這就是為什麼他們相互移動,但彼此距離不遠。
6.讓學生在分子水平上繪製自己的水模型和完成活動表。
繪製或投影插圖水分子
www.middleschoolchemistry.com/multimedia/chapter1/lesson1#water_molecules
向學生解釋這是一個水分子模型。指出這些分子沒有任何確切的順序,但彼此靠近。它們有一彎曲的“運動線”來顯示分子正在移動。讓學生在他們的活動表單上繪製分子水平的模型。他們應該使用之前教學者顯示的模型來做為引導。
學生的圖畫應該顯示分子是:
- 隨機排列
- 因為彼此吸引,所以彼此靠近
- 相互移動但不能分開
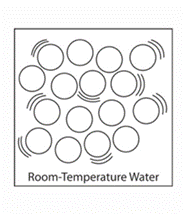
圖五繪圖顯示分子運動方式
確保學生認識到這個模型顯示的水分子比實際上大得多。水分子不僅體積小,它們的數量也非常多。一滴水是由超過十億億個極小的水分子所組成。
為了讓學生了解水分子是多麼小,你可以告訴學生以下幾點:在大約1湯匙的水裡,大約有6000億億個水分子。如果你能每秒鐘計算一百萬個水分子,那就需要大約2億年的時間才能計算出一大湯匙水中的所有分子。原子和分子數量巨大,規模卻小得令人難以置信。
l 延伸
7.展示影片,讓學生看到一個水分子互相吸引的例子
顯示慢動作彈出的水氣球的影片。
www.middleschoolchemistry.com/multimedia/chapter1/lesson1#water_balloon
詢問學生
•你為什麼認為在氣球爆裂的時候,水保持了它的形狀?
學生們應該意識到,水很好地保持在一起,因為水分子是相互吸引的。
•想像一下,你的手指上掛著一滴水。氣球彈出後,這與水一起怎麼樣?
這也可以藉由水分子彼此間極具引力的現象來解釋。
額外的延伸
如果你有時間,讓學生有機會玩水滴遊戲。
1.水滴,團結力量大(見附錄三)
教師準備
給每組2張「團結力量大」表。
程序
(1) 把一張蠟紙粘在「團結力量大」表上。
(2) 在外面的每個小圓圈裡放5滴水。
(3) 盡快地用你的吸管將每一個小圈裡的水滴拖到中心的大圓圈裡。當所有水滴都聚集在大圓圈裡,就表示你完成了。
(4) 挑戰你的伙伴,看看誰能最快地把所有的水滴團結在一起。
2.水珠競速比賽(見附錄四)
教師準備
為每組準備2張水珠競速比賽(Race Drop Raceway)表。你和夥伴可以跟著下面的方向來和對方比賽。
程序
1. 將“Race Drop Raceway”表單放在一張硬紙板上加以固定。
2. 在“Race Drop Raceway”表單上粘上一張蠟紙。
3. 在「開始」處滴上2-4滴水,讓它成為一個較大的水滴。
4. 把紙板傾斜,引導表單上的水滴沿著賽道盡快的滾落到「終點」處。盡量不要碰
到賽道的邊緣,最快完成的便是勝利者。
參、綜合活動
■學生課程回饋單
筆者在學習單背面設計了一份問卷,調查學生對此次實驗與活動的看法及收獲,回答問卷的六年級學生共28人,男15人、女13人,問題與摘錄如下。
問題1你對這個活動所感受到的喜愛程度如何?
表二:學生回答問題的答案統計
|
選項
|
非常喜歡
|
有點喜歡
|
普通
|
不太喜歡
|
非常不喜歡
|
|
人數
|
18
|
9
|
1
|
0
|
0
|
|
比率
|
64.29%
|
32.14%
|
3.57%
|
0%
|
0%
|
由表一可知道,有64.29%的學生在教學活動結束後,對於此課程的感受是「非常喜歡」,32.14%感到「有點喜歡」,有1位學生回應喜愛程度「普通」,因為這位學生對這個活動沒有那麼感興趣的緣故。因此,整體而言,對六年級的學生而言,這樣的課程設計是他們能夠接受而且是受到喜愛的。
問題2 承上題,為什麼你會勾這個選項?因為…
根據參與學童的問卷回饋,他們之所以會勾選喜歡的原因是對課程活動感到好玩、可以競賽和玩遊戲,對於日常隨處可見的水珠竟然有不易分開卻可以輕易的聚合在一起的現象感到很新奇。本次進行實驗的學生班級共有28位學生,以S01~S28為代號,摘錄幾位同學特別的學習感受,分享給大家(如下所示)。
S02:有點喜歡,因為我喜歡自然科的活動,而且很好玩。
S06:非常喜歡,因為我覺得這些水珠的實驗很有趣。
S10:非常喜歡,因為我覺得這個活動是在生活中不難見到的,但是卻沒有深入瞭解。
S11:非常喜歡,因為水分子的活動在家裡也可以玩。
S14:有點喜歡,因為活動中的遊戲很好玩。
S15:有點喜歡,因為我覺得水有很多種變化,令人感到有趣。
S21:非常喜歡,因為我本來就喜歡觀察水分子。
S25:非常喜歡,因為我覺得這個活動很好玩,可以競賽和玩遊戲。
S27:非常喜歡,因為它很有趣又可以學到豐富的知識,我喜歡這樣的課程。
S28:非常喜歡,因為覺得這活動非常棒,讓我增加很多知識。
問題3 在這次的課程中,你學到了什麼?
課程結束後,學生是否學習到課程中的核心概念,是教學者設計課程的主要目標,本次進行課程的學生學到了什麼,根據參與學童的問卷回答,他們在課程活動中的主要學習收穫是了解如何利用水分子的拆分、聚合來理解物質是由極小的粒子所組成;水分子會碰撞產生運動,因此物質中的粒子也可以運動。筆者摘錄如下:
S02:我學到了水分子的特性。
S06:水珠的分子會因為相互碰撞,而分開。
S10:我學到了水分子的運動和特性。
S11:我學到了水滴聚在一起是容易的。
S14:我學到了:1.水分子的運動2.水分子會互相吸引3.水分子有擴散的性質。
S15:我學到水分子會互相聚集,所以氣球破掉時,水會維持一樣的形狀。
S21:水分子的碰撞和路線,和水不容易分散。
S25:我學到了水分子容易聚集且不易分散,還有水分子會運動。
S27:我學到水分子易聚合但不易分散。
S28:我學到了原來水很難拆分,但很容易加入在一起。

圖六學生填寫課程回饋單
■教師的教學省思
經由學生們在完成上述課程後所填寫的課程回饋單,讓筆者可以了解學生們心中對此課程活動的真實想法。只要能結合他們的生活經驗、有趣又能動手做的課程,即使是用問答式的課程內容來進行教學,學生也能透過實際的操作、觀察與紀錄來了解教材內容所欲傳達的知識。在自然科學課程當中多給與學生實際動手做的教學方式會比講述式的教學來得活潑有趣,較能吸引學生的注意力,也更能讓學生體悟「做中學」的重要性,對於提升學生的學習成效是有助益的。
在現代科技一日千里的今天,身為老師的我們,不能只單靠一本教科書或者是一本教師手冊來進行教學活動,我們應該善加運用影音媒體或電腦科技,讓一些不易在課堂上呈現的現象或實驗結果可以透過影片、動畫、互動式的教學媒材,具體的呈現在學生眼前,幫助他們去了解、去分析課程內容所欲傳達的知識,甚至能激勵學生們做更進一步的探究。
■課程實施過程及注意事項
一、本次主要課程活動設計大約需一節課的時間,在進行探索活動前先發下活動紀錄表給學生,讓學生能對此活動實施的目的、步驟與要觀察的事物加以瞭解,並在活動過程中詳實記錄下所看到的現象。
二、因為在進行此實驗前尚無法取得蠟紙(wax paper),故而此實驗中的蠟紙先以塑膠膜暫代(水滴可在膠膜上移動);為了避免紙張受潮,已在課前事先將各種表單加以護貝;為了易於觀察水滴在紙上的移動情形,因此以藍色紙張來印製表單。
三、因為室溫中的水滴是透明無色的,不易觀察它的各種變化,因此,事先在水裡添加紅色顏料,讓學生容易看到滴管中擠出的水滴形態與水滴在表單上的移動情形。
四、筆者試著利用五種不同材質的紙張來進行水滴移動及分合的活動,結果發現,效果最佳的是蠟光紙,水滴在蠟光紙上可以輕易移動與進行分合,不易留下水漬;其次是烘焙紙,易讓水滴移動與分合,但容易留下水漬;至於表面有覆膜的牛皮紙、卡典西德紙(膠膜)及護貝過的紙,雖然不會被滲透,但容易在移動過程中留下水痕,因此水滴移動與分合的實驗成效不如使用蠟光紙和烘焙紙(圖七~圖十)。
|

|

|
|
圖七:實驗前
|
圖八:進行實驗中
|
|

|

|
|
圖九:進行實驗中
|
圖十:實驗後
|
■結語
很高興能順利的在自己的教學課堂上完成這個課程,雖然目前只有在一個班級中實施。但能看到學生們驚奇且樂於學習的表情,也讓我備感欣慰。誠如S10學生所言:這個活動是在生活中不難見到的,但是卻沒有深入瞭解,期望藉由此課程的進行能讓同學們了解到生活中處處皆科學的道理。
■參考資料
1.教育部(2017)。十二年國教自然科學領域課程手冊(初稿)。2018年 1月15日,取自:
https://www.naer.edu.tw/ezfiles/0/1000/img/67/196757124.pdf
2.美國中學化學教材。2018年 1月14日,取自:
http://www.middleschoolchemistry.com/lessonplans/chapter1/lesson1
3.信望愛文教基金會(2017)。項少龍老師物理1進階講義。2017年12月29日,取自:
https://www.learnmode.net/flip/book_reader/423
4.2017年12月29日,取自:
http://enjoy.phy.ntnu.edu.tw/mod/resource/view.php?id=20561
5. 康軒書局(2016)。國民小學自然與生科技教師手冊第七冊(第三版)。臺北市:康軒。
■謝誌
在此感謝國立臺北教育大學自然科學教育學系106學年度第1學期化學特論(一)周金城教授與全體同學協助,提供本文架構調整與內文修正之意見,讓本文可以更好,在此謹深摯謝忱。
「附錄」